IBRITUMOMAB TIUXETAN
AMM / Liste I / Hors GHS (T2A).
Présentation(s)
ZEVALIN - 1,6 MG / ML
Forme(s) galénique(s)
Trousse pour préparation radio-pharmaceutique, présentée sous forme d'une boîte comprenant 4 flacons :
- un flacon de 2 mL de solution d'ibritumomab tiuxétan (3,2 mg d’ibritumomab tiuxétan, chlorure de sodium, eau PPI) ;
- 2 flacons d’excipients : 1 flacon de 2 mL d'acétate de sodium (acétate de sodium, eau PPI), 1 flacon de 10 mL de solution tampon (solution d’albumine humaine, chlorure de sodium, phosphate disodique dodécahydraté, hydroxyde de sodium, phosphate monopotassique, chlorure de potassium, acide pentétique, acide chlorhydrique dilué, eau PPI),
- 1 flacon vide de réaction de 10 mL.
Renseignements physico-chimiques
Trousse à radiomarquer par le chlorure d'Yttrium 90 :
- Ibritumomab : anticorps monoclonal anti-CD20 murin de type IgG1 kappa recombinant, produit par génie génétique à partir de cellules ovariennes de hamster chinois (CHO),
- Tiuxétan (MX-DTPA) : chélateur de l’yttrium 90,
- Yttrium 90 : radionucléide émetteur de particules bêta moins d’énergie élevée (se reporter à la monographie Yttrium 90 (Chlorure) pour les renseignements physiques).
L’ibritumomab est lié par liaison covalente au tiuxétan.
Préparation / Conservation
Recommandations des laboratoires pharmaceutiques
Spécialité(s)
Conservation
- de la trousse : entre +2°C et +8°C, à l'abri de la lumière, dans le conditionnement primaire.
- de la préparation radiopharmaceutique après radiomarquage : entre +2°C et +8°C, le flacon étant placé dans une protection blindée appropriée.
Stabilité
- de la trousse : 4 ans.
- de la préparation radiopharmaceutique après radiomarquage : 8 heures mais utilisation immédiate recommandée.
Solution(s) reconstituée(s)
Préparation radiopharmaceutique
- Mode opératoire
Pendant toute la préparation, respecter les règles d'asepsie et de radioprotection (cf. tableau I).
Avant l’administration, déterminer la pureté radiochimique (PRC) de la préparation radiopharmaceutique. Ne pas administrer si la PRC moyenne est < à 95 %.
Tableau I. Préparation de l’ibritumomab tiuxétan marqué par le chlorure d’yttrium [90Y].
| Mettre la trousse à température ambiante | Avant le début du radiomarquage (au moins 1 heure) |
| Effectuer tous les calculs avant de commencer le radiomarquage | V1 : volume de chlorure d’Yttrium 90 contenant 1500 MBq V2 : volume d’acétate de sodium = 1,2 x V1 1,3 mL d’ibritumomab tiuxétan VT : volume totale de réaction = V1 + V2 + 1,3 mL V3 : 10 mL - VT |
Désinfecter les bouchons des 4 flacons de la trousse et du flacon de chlorure d’yttrium [90Y] | |
| Prélever aseptiquement | V2 d’acétate de sodium à l’aide d’une seringue stérile de 1 mL munie d’une aiguille (20-21G) 1,3 mL d’ibritumomab tiuxétan à l’aide d’une seringue stérile de 2-3 mL munie d’une aiguille (20-21G) V3 de solution tampon à l’aide d’une seringue stérile de 10 mL munie d’une aiguille (18-20G), en utilisant éventuellement une aiguille de mise à l’air V1 de chlorure d’yttrium [90Y] (1500 MBq), dans l’enceinte blindée |
| Radiomarquage, dans l’enceinte blindée, en effectuant les étapes impérativement dans l’ordre suivant : | - placer le flacon de réaction dans une protection blindée appropriée, - injecter dans le flacon de réaction l’acétate de sodium puis le chlorure d’yttrium [90Y], - mélanger doucement, - injecter dans le flacon de réaction les 1,3 mL d’ibritumomab tiuxétan, mélanger doucement en évitant la formation de mousse puis déclencher le chronomètre, - laisser incuber 5 ± 1 min à température ambiante (temps d’incubation obligatoirement entre 4 et 6 min), - pour arrêter la réaction, injecter dans le flacon de réaction la solution tampon (en la faisant couler doucement le long des parois pour éviter la formation de mousse) et mélanger doucement. |
| Facultatif : | Une aiguille de mise à l’air peut être placée : - soit juste avant l’injection du chlorure d’yttrium [90Y], - soit juste avant l’injection de la solution tampon. |
- Forme(s) galénique(s) obtenue
Solution injectable pour perfusion
Contrôle
- Caractères organoleptiques
Solution limpide, légèrement jaune.
- Pureté radiochimique
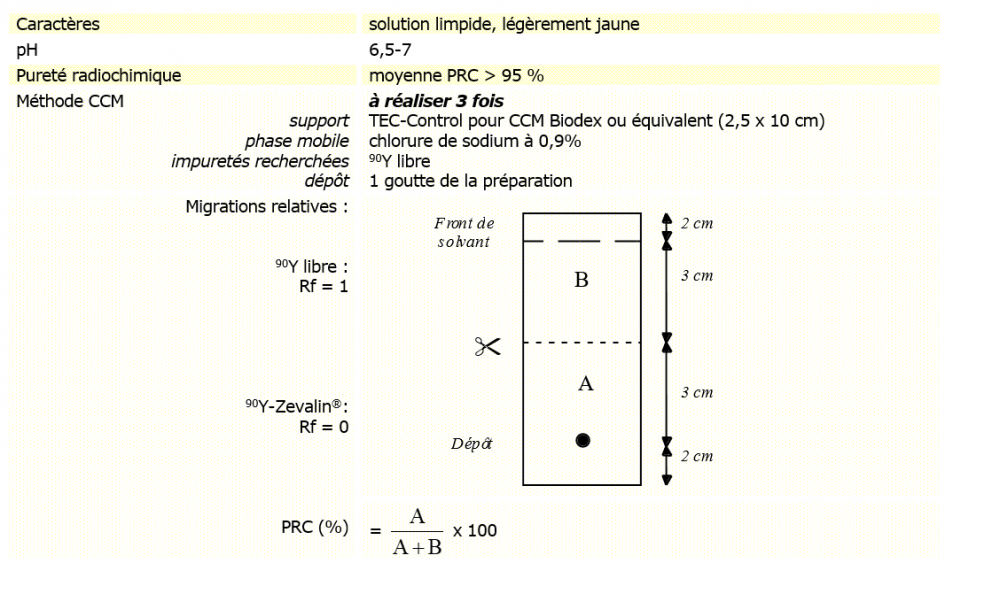
Réaliser 3 fois la même chromatographie couche mince (CCM) selon la méthode indiquée dans le tableau II. Plusieurs méthodes de mesure d’activité de la CCM peuvent être utilisées.
Tableau II. Contrôle physico-chimique du 90Y-Zevalin®
Recommandations de la SoFRa
La SoFRa recommande cette méthode de CQ validée et publiée : …
Propriétés pharmacologiques
Mécanisme d'action
L'ibritumomab tiuxétan est un anticorps monoclonal murin de type IgG1 kappa recombinant, spécifique de l'antigène CD20 situé à la surface des lymphocytes B, tant malins que normaux.
L'ibritumomab tiuxétan marqué à l'yttrium 90 ([90Y]-Zevalin®) se lie spécifiquement aux lymphocytes B, y compris les cellules malignes, exprimant l'antigène CD20.
Les effets cellulaires sont liés à l’irradiation par les rayonnements de l'Yttrium 90, radionucléide émetteur bêta moins pur. Le parcours maximum des particules bêta moins libérées est d’environ 11 mm dans les tissus et 90% de l’énergie émise sont absorbés sur 5 mm.
Les administrations préalables de rituximab (Mabthéra®), à concen-tration infrathérapeutique (250 mg/m2), permettent d’éliminer les lymphocytes B circulants et d’améliorer la sélectivité tumorale de l'ibritumomab tiuxétan radiomarqué.
Le traitement par [90Y]-Zevalin® entraîne également une diminution des lymphocytes B CD20+ normaux mais ce phénomène n'est que temporaire. La récupération des lymphocytes B commence dans les 6 mois suivant le traitement (avec une médiane se situant à nouveau dans les limites de la normale dans les 9 mois suivant le traitement).
Pharmacocinétique
Chez des malades recevant des perfusions intraveineuses de 250 mg/m2 de rituximab, suivies d'injections intraveineuses de 15 MBq/kg de [90Y]-Zevalin®, la période effective médiane de [90Y]- Zevalin® a été de 28 heures.
La biodistribution de [90Y]-Zevalin® suit celle de l’anticorps, l’yttrium 90 formant un complexe stable avec l'ibritumomab tiuxétan.
Seulement environ 6% de la dose injectée est éliminée par voie urinaire, dont 70% dans les 4 premiers jours.
Dosimétrie
Des études dosimétriques du Zevalin® marqué à l’Indium 111 ont été réalisées pour estimer la dose d’irradiation des différents organes après administration de [90Y]-Zevalin®.
Estimation des doses absorbées après administration de [90Y]-Zevalin®.
| Organes critiques | mGy/MBq | |
| Médiane | Extrêmes | |
| Rate | 9,4 | 1,8 – 20,0 |
| Foie | 4,8 | 2,9 – 8,1 |
Paroi inférieure du gros intestin | 4,7 | 3,1 – 8,2 |
Paroi supérieure du gros intestin | 3,6 | 2,0 – 6,7 |
| Paroi cardiaque | 2,9 | 1,5 – 3,2 |
| Poumons | 2,0 | 1,2 – 3,4 |
| Testicules | 1,5 | 1,0 – 4,3 |
| Intestin grêle | 1,4 | 0,8 – 2,1 |
| Moelle rouge | 1,3 | 0,7 – 1,8 |
| Paroi de la vessie | 0,9 | 0,7 – 1,3 |
| Surfaces osseuses | 0,9 | 0,5 – 1,2 |
| Ovaires | 0,4 | 0,3 – 0,5 |
| Utérus | 0,4 | 0,3 – 0,5 |
| Thyroïde | 0,3 | 0,2 – 0,5 |
| Reins | 0,1 | 0,0 – 0,3 |
| Corps entier | 0,5 | 0,4 – 0,7 |
Indications / Utilisation
- LES - I000387 Marqué à l’yttrium-90 traitement de consolidation après induction d’une rémission chez les patients atteints d’un lymphome folliculaire non traités antérieurement. Les bénéfices de Zevalin suite à l’utilisation du rituximab associé à une chimiothérapie n’ont pas été démontrés.
- LES - I000388 Marqué à l'yttrium-90 traitement des patients adultes atteints d’un lymphome non hodgkinien (LNH) à cellules B CD20+, de type folliculaire, en rechute ou réfractaire après traitement par le rituximab.
- NA
AMM
L'ibritumomab tiuxétan marqué à l'yttrium 90 est indiqué :
- dans le traitement des malades adultes atteints d’un lymphome non hodgkinien (LNH) à cellules B CD20 positif, de type folliculaire, en rechute ou réfractaire après traitement par le rituximab(Code LES I000388).
- dans le traitement de consolidation après induction d’une rémission chez les malades atteints d’un lymphome folliculaire non traités antérieurement (Code LES I000387).
Autres études
HORS AMM
- Conditionnement d’intensification thérapeutique dans le traitement des lymphomes
L’utilisation de [90Y]-Zevalin® dans cette indication a fait l’objet de protocoles cliniques. Dans une étude de phase II (55), le conditionnement par [90Y]-Zevalin® et fludarabine lors d’une transplantation de cellules hématopoïétiques chez des malades atteints d’un lymphome permet d’obtenir un taux de survie à 2 ans de 51%.
Dans une autre étude portant sur 19 malades (56), le conditionnement par [90Y]-Zevalin® / busulfan / cyclophosphamide / étoposide apporte un taux de réponse globale de 84.2% et une survie globale à 3 ans de 52.6%.
Les bénéfices de [90Y]-Zevalin® suite à l’utilisation du rituximab associé à une chimiothérapie n’ont pas été démontrés.
Mode d'administration / Posologies
Mode d'administration
- Préparation du malade
- Le [90Y]-Zevalin® est utilisé après prétraitement par le rituximab.
Ce prétraitement est effectué sur une période de 8 jours. Il consiste en deux administrations intraveineuses de rituximab selon le schéma suivant :
- J1 : perfusion IV de rituximab (250 mg/m2),
- J7, J8 ou J9 : perfusion IV de rituximab (250 mg/m2) brève (moins de 4 heures) avant la perfusion IV de [90Y]-Zevalin®.
- Mode d’administration
L'ibritumomab tiuxétan marqué à l'yttrium 90 ([90Y]-Zevalin®) est
administré par perfusion intra-veineuse lente pendant 10 minutes. Ne pas administrer en bolus intraveineux. Il est recommandé d’utiliser une seringue placée dans un pousse seringue, lui-même placé derrière un écran adapté (type plexiglas).
Le [90Y]-Zevalin® peut être directement injecté dans la tubulure après avoir arrêté la perfusion IV. La tubulure doit comporter un filtre de 0,2 ou 0,22 microns, à faible liaison protéique, entre le malade et le robinet permettant l’injection. Rincer la tubulure avec au moins 10 mL de sérum physiologique à 0,9 % après la perfusion de [90Y]-Zevalin®.
Le malade peut être traité en hôpital de jour. Un isolement en chambre protégée n’est pas nécessaire, le malade peut rentrer chez lui après quelques heures d’observation.
Posologies
Le [90Y]-Zevalin® est utilisé après prétraitement par le rituximab :
J7, J8 ou J9 : perfusion intraveineuse de [90Y]-Zevalin®, après la perfusion intraveineuse de rituximab.
La posologie de [90Y]-Zevalin® est calculée selon la numération plaquettaire avant traitement.
Chez les malades recevant [90Y]-Zevalin® en monothérapie :
- en cas de numération plaquettaire ≥ 150 000/mm3 : 15 MBq/kg, sans dépasser 1200 MBq,
- en cas de numération plaquettaire comprise entre 100 000 et 150 000 par mm3 : 11 MBq/kg, sans dépasser 1 200 MBq.
- en cas de numération plaquettaire < 100 000 par mm3 : ne pas l’utiliser.
Lorsque [90Y]-Zevalin® est utilisé en traitement de consolidation :
- en cas de numération plaquettaire ≥ 150 000/mm3 : 15 MBq/kg, sans dépasser 1 200 MBq,
- en cas de numération plaquettaire < 150 000 par mm3 : ne pas l’utiliser.
On ne dispose pas de données sur l'utilisation réitérée de [90Y]-Zevalin®.
Contre-indications / Précautions d'emploi
Contre-indication
- Grossesse et allaitement.
- Hypersensibilité à l’ibritumomab tiuxétan, au chlorure d’yttrium, aux autres protéines d’origine murine ou à l’un des excipients.
Précautions d'emploi
- Ne pas administrer aux malades susceptibles de présenter des signes de toxicité hématologique menaçant leur pronostic vital.
- Ne pas administrer chez les malades suivants, car efficacité et tolérance non établies :
- malades chez qui l’envahissement médullaire par les cellules lymphomateuses est > à 25 %,
- malades préalablement soumis à une irradiation externe affectant plus de 25 % de la moelle osseuse active,
- malades recevant [90Y]-Zevalin® en monothérapie et dont la numération plaquettaire est <100 000/mm3 et malades recevant [90Y]-Zevalin® en traitement de consolidation après induction d’une rémission et dont la numération plaquettaire est < 150 000/mm3,
- malades présentant une numération de polynucléaires neutrophiles < 1500/mm3,
- malades ayant reçu une greffe de moelle osseuse ou de cellules souches.
- Administration déconseillée chez les enfants et adolescents de moins de 18 ans (absence de données concernant la sécurité et l’efficacité).
- Administration déconseillée chez les malades présentant un LNH avec atteinte du SNC (absence de données chez ce type de malades).
- Ne pas administrer de traitement par un facteur de croissance de type G-CSF dans les 3 semaines précédant le traitement par [90Y]-Zevalin® ainsi que pendant les 2 semaines suivant la fin du traitement, en raison de la possible sensibilité des cellules myéloïdes à division rapide aux radiations.
- Des précautions sont à prendre en cas d’insuffisance médullaire.
- Chez la plupart des malades, l’administration de [90Y]-Zevalin® (après prétraitement par le rituxi-mab) entraîne une cytopénie sévère et prolongée qui est généralement réversible. Par conséquent, après l'administration de [90Y]-Zevalin®, réaliser un suivi hebdomadaire des numérations sanguine et plaquettaire. Le risque de toxicité hémato-logique peut être augmenté après un traitement préalable contenant de la fludarabine.
- Rechercher des anticorps humains anti-souris (HAMA) chez les malades ayant reçu des anticorps murins avant [90Y]-Zevalin®.
- Après administration de [90Y]-Zevalin®, rechercher des anticorps humains anti-souris (HAMA) chez les malades avant toute nouvelle administration de protéines d’origine murine.
- Pendant la semaine qui suit l’administration de [90Y]-Zevalin®, le malade devra éviter le contact prolongé et rapproché avec les jeunes enfants et les femmes enceintes, veiller à se laver soigneusement les mains après chaque miction et utiliser des préservatifs.
- Ce médicament peut contenir jusqu’à 28 mg de sodium par dose, en fonction de la concentration radioactive. A prendre en compte chez les malades contrôlant leur apport alimentaire en sodium.
- La sécurité et l’efficacité n’ont été étudiées ni chez les malades présentant une insuffisance rénale, ni chez les malades présentant une insuffisance hépatique.
- Une contraception efficace doit être utilisée par les femmes susceptibles de procréer et les hommes pendant l'administration de [90Y]-Zevalin® et jusqu’à 12 mois après le traitement.
Effets indésirables
Effets indésirables
| Organe / Effet indésirable | Fréquence | Grade | Caractères - Surveillance - Prévention |
|---|---|---|---|
| TROUBLES DE LA PEAU ET DES APPENDICES | |||
|
PRURIT
RASH CUTANE |
|||
| TROUBLES DES FONCTIONS SEXUELLES | |||
|
AMENORRHEE
|
|||
| TROUBLES DE LA PEAU ET DES APPENDICES | |||
|
PRURIT
RASH CUTANE |
|||
| TROUBLES DES FONCTIONS SEXUELLES | |||
|
AMENORRHEE
|
|||
| TROUBLES DE LA PEAU ET DES APPENDICES | |||
|
PRURIT
RASH CUTANE |
|||
| TROUBLES DES FONCTIONS SEXUELLES | |||
|
AMENORRHEE
|
|||
| HYPERSENSIBILITE | Réactions d’hypersensibilité sévères (grade 3/4), dont une anaphylaxie, ont été décrites chez moins de 1 % des malades. Des médicaments permettant de traiter ces réactions d’hypersensibilité (adrénaline, antihistaminiques, corticoïdes…) doivent être disponibles pour administration immédiate en cas de réaction allergique au cours de l’administration de [90Y]-Zevalin®. |
||
| FREQUENT | G3 G4 | ||
| TROUBLES HEMATOLOGIQUES | Une toxicité hématologique dose-limitante est très souvent rapportée dans les essais cliniques. Le délai médian de survenue du nadir des plaquettes et des polynucléaires a été de 60 jours environ après le début du traitement. - Indication LNH en rechute et réfractaire : le délai médian de récupération des thrombopénies de grade 3 ou 4 a été de 13 et 21 jours, celui des neutropénies de grade 3 ou 4 de 8 et 14 jours. - Traitement de consolidation : le délai médian de récupération des thrombopénies de grade 3 ou 4 a été de 20 et 35 jours et celui des neutropénies de grade 3 ou 4 de 20 et 28 jours. |
||
|
NEUTROPENIE
THROMBOPENIE ANEMIE HYPERLEUCOCYTOSE |
TRES FREQUENT | ||
|
PANCYTOPENIE
LYMPHOPENIE NEUTROPENIE FEBRILE |
FREQUENT | ||
| TROUBLES IMMUNOLOGIQUES | - Indication LNH en rechute et réfractaire : Infections de grade 3 et 4 fréquentes au cours des 13 premières semaines de traitement par [90Y]-Zevalin®. Infections de grade 3 fréquentes au cours de la période de suivi, grade 4 peu fréquent. - Traitement de consolidation : Infections fréquemment observées, pouvant être bactériennes, fongiques ou virales. |
||
|
INFECTION
|
TRES FREQUENT | ||
|
SEPTICEMIE
INFECTION URINAIRE PNEUMONIE CANDIDOSE ORALE |
FREQUENT | ||
| SECOND CANCER | Des cas de myélodysplasies / leucémies aiguës lymphocytaires ont été rapportés chez 5 malades sur 211 traités par [90Y]-Zevalin®. L’imputabilité du [90Y]-Zevalin® a été difficile à déterminer, ces malades ayant reçu précédemment des agents alkylants. |
||
|
SYNDROME MYELODYSPLASIQUE
LEUCEMIE AIGUE MYELOIDE DOULEUR TUMORALE |
FREQUENT | ||
| TROUBLES LOCAUX | Des cas d’extravasation avec réaction ultérieure au site de perfusion ont été rapportés (dermatite, desquamation, ulcère) Une étroite surveillance à la recherche de signes d’extravasation lors de l’injection de [90Y]-Zevalin® est nécessaire. Au moindre signe ou symptôme d’extravasation, la perfusion doit être immédiatement arrêtée et reprise dans une autre veine. |
||
|
REACTION AU SITE D’INJECTION
|
|||
| TROUBLES GASTRO-INTESTINAUX | |||
|
NAUSEES
|
TRES FREQUENT | ||
|
DIARRHEE
DOULEUR ABDOMINALE VOMISSEMENT CONSTIPATION DYSPEPSIE IRRITATION DE LA GORGE |
FREQUENT | ||
| TROUBLES GENERAUX | |||
|
FRISSONS
FATIGUE/ASTHENIE FIEVRE/HYPERTHERMIE |
TRES FREQUENT | ||
|
DOULEUR
OEDEME PERIPHERIQUE SYNDROME GRIPPAL MALAISE HYPERHIDROSE / HYPERSUDATION |
FREQUENT | ||
| TROUBLES CARDIO-VASCULAIRES | |||
|
PETECHIE
|
TRES FREQUENT | ||
|
HYPERTENSION ARTERIELLE
HYPOTENSION ARTERIELLE HEMORRAGIE |
FREQUENT | Hémorragies secondaires à une thrombocytopénie. |
|
| TROUBLES METABOLISME ET NUTRITION | |||
|
ANOREXIE
|
FREQUENT | ||
| TROUBLES MUSCULO-SQUELETTIQUES | |||
|
ARTHRALGIE
MYALGIE DOULEUR DORSALE CERVICALGIE |
FREQUENT | ||
| TROUBLES NEUROLOGIQUES | |||
|
CEPHALEES
SENSATION D'EBRIETE |
FREQUENT | ||
|
INSOMNIE
ANXIETE |
FREQUENT | ||
| TROUBLES RESPIRATOIRES | |||
|
TOUX
RHINITE |
|||
Interactions médicamenteuses
Intéractions médicamenteuses
Les interactions médicamenteuses sont regroupées et traitées dans le chapitre spécifique Interactions médicamenteuses significatives.
Généralités / Annexes / Protocoles associés
Auteurs
Références bibliographiques
2. Bethge WA, Lange T, Meisner C et al. Radioimmunotherapy with yttrium-90-ibritumomab tiuxetan as part of a reduced- intensity conditioning regimen for allogeneic hematopoietic cell transplantation in patients with advanced non-Hodgkin lymphoma: results of a phase 2 study. Blood. 2010 Sep 9;116(10):1795-802. doi: 10.1182/blood-2010-02-270538. Epub 2010 Jun 7. PMID: 20530284. (https://pubmed.ncbi.nlm.nih.gov/20530284/)
3. Borghaei H, Schilder RJ. Safety and efficacy of radioimmunotherapy with yttrium 90 ibritumomab tiuxetan (Zevalin). Semin Nucl Med. 2004 Jan;34(1 Suppl 1):4-9. doi: 10.1053/j.semnuclmed.2003.11.002. PMID: 14762738. (https://pubmed.ncbi.nlm.nih.gov/14762738/)
4. Bourrel F. Utilisation de l’ibritumomab tiuxétan marqué à l’yttrium-90 dans le traitement des lymphomes non hodgkiniens à cellules B. Actualités pharma ()
5. Kang BW, Kim WS, Kim C et al. Yttrium-90-ibritumomab tiuxetan in combination with intravenous busulfan, cyclophosphamide, and etoposide followed by autologous stem cell transplantation in patients with relapsed or refractory B-cell non-Hodgkin's lymphoma. Invest New Drugs. 2010 Aug;28(4):516-22. doi: 10.1007/s10637-009-9283-z. Epub 2009 Jun 23. PMID: 19547918. (https://pubmed.ncbi.nlm.nih.gov/19547918/)
6. Nademanee A, Forman S, Molina A, et al. A phase 1/2 trial of high-dose yttrium-90-ibritumomab tiuxetan in combination with high-dose etoposide and cyclophosphamide followed by autologous stem cell transplantation in patients with poor-risk or relapsed non-Hodgkin lymphoma. Blood. 2005 Oct 15;106(8):2896-902. doi: 10.1182/blood-2005-03-1310. Epub 2005 Jul 7. PMID: 16002426; PMCID: PMC1895300. (https://pubmed.ncbi.nlm.nih.gov/16002426/)
7. O'Brien LM, Waight CC, Millar AM. A comparison of techniques for analysing 90Y-Zevalin thin-layer chromatography plates. Nucl Med Commun. 2005;26(2):163-166. doi:10.1097/00006231-200502000-00014 (https://pubmed.ncbi.nlm.nih.gov/15657511/)
8. Rizzo-Padoin N. Apport de la radio-immunothérapie au traitement des lymphomes [Contribution of radioimmunotherapy to the treatment of lymphoma]. Ann Pharm Fr. 2008;66(5-6):300-308. doi:10.1016/j.pharma.2008.09.003. (https://pubmed.ncbi.nlm.nih.gov/19061730/)
9. Shah J, Wang W, Harrough VD et al. Retreatment with yttrium-90 ibritumomab tiuxetan in patients with B-cell non-Hodgkin's lymphoma. Leuk Lymphoma. 2007 Sep;48(9):1736-44. doi: 10.1080/10428190701528517. PMID: 17786709. (https://pubmed.ncbi.nlm.nih.gov/17786709/)
10. Shimoni A, Zwas ST, Oksman Y, et al. Ibritumomab tiuxetan (Zevalin) combined with reduced-intensity conditioning and allogeneic stem-cell transplantation (SCT) in patients with chemorefractory non-Hodgkin's lymphoma. Bone Marrow Transplant. 2008;41(4):355-361. doi:10.1038/sj.bmt.1705919. (https://pubmed.ncbi.nlm.nih.gov/18026153/)
11. Spies SM. Imaging and dosing in radioimmunotherapy with yttrium 90 ibritumomab tiuxetan (Zevalin). Semin Nucl Med. 2004 Jan;34(1 Suppl 1):10-3. doi: 10.1053/j.semnuclmed.2003.11.004. PMID: 14762739. (https://pubmed.ncbi.nlm.nih.gov/14762739/)
12. Tennvall J, Fischer M, Bischof Delaloye A, et al. EANM procedure guideline for radio-immunotherapy for B-cell lymphoma with 90Y-radiolabelled ibritumomab tiuxetan (Zevalin). Eur J Nucl Med Mol Imaging. 2007;34(4):616-622. doi:10.1007/s00259-007-0372-y. (https://pubmed.ncbi.nlm.nih.gov/17323056/)
13. Urbano N, Modoni S. Evaluation of different beta-counting systems involved in 90Y-Zevalin quality control. Nucl Med Commun. 2007;28(12):943-950. doi:10.1097/MNM.0b013e3282f1ac59 (https://pubmed.ncbi.nlm.nih.gov/18090222/)
14. Wiseman GA, Witzig TE. Yttrium-90 (90Y) ibritumomab tiuxetan (Zevalin) induces long-term durable responses in patients with relapsed or refractory B-Cell non-Hodgkin's lymphoma. Cancer Biother Radiopharm. 2005;20(2):185-188. doi:10.1089/cbr.2005.20.185. (https://pubmed.ncbi.nlm.nih.gov/15869453/)
15. Wiseman GA, White CA, Sparks RB, et al. Biodistribution and dosimetry results from a phase III prospectively randomized controlled trial of Zevalin radioimmunotherapy for low-grade, follicular, or transformed B-cell non-Hodgkin's lymphoma. Crit Rev Oncol Hematol. 2001;39(1-2):181-194. doi:10.1016/s1040-8428(01)00107-x. (https://pubmed.ncbi.nlm.nih.gov/11418315/)
16. Witzig TE, White CA, Gordon LI et al. Safety of yttrium-90 ibritumomab tiuxetan radioimmunotherapy for relapsed low-grade, follicular, or transformed non-hodgkin's lymphoma. J Clin Oncol. 2003 Apr 1;21(7):1263-70. doi: 10.1200/JCO.2003.08.043. PMID: 12663713. (https://pubmed.ncbi.nlm.nih.gov/12663713/)
17. RCP : ZEVALIN (https://www.ema.europa.eu/documents/product-information/zevalin-epar-product-information_fr.pdf)


